خريطة جينية ثورية تُبشر بكشف أسرار الزهايمر
دراسة غير مسبوقة تحدد 'محاور جينية' قد تغير مسار العلاج
كشفت دراسة حديثة عن خريطة جينية هي الأولى من نوعها، واعدةً بفك شفرات تسلسل الأسباب والنتائج لنشاط الجينات التي يُعتقد أنها تقود المرض داخل الدماغ. هذه الخريطة، التي تُعدّ سابقة فريدة، لا تكتفي برصد لقطات لنشاط الجينات في خلايا دماغية محددة فحسب، بل تُظهر أيضاً الروابط بين الجينات، كاشفةً عن مسارات محتملة لتفاعلات متسلسلة.
وعبر هذه الرؤية الجديدة، تمكن فريق البحث من جامعتي كاليفورنيا في إيرفين (UC Irvine) وبيردو بالولايات المتحدة، من تحديد ما أطلقوا عليه “المحاور الجينية” (hub genes)، وهي نقاط التقاء رئيسية لنشاط الجينات، وقد تُصبح أهدافاً واعدة لعلاجات ألزهايمر المستقبلية.
وتوضح الدكتورة مين تشانغ، عالمة الأوبئة في جامعة كاليفورنيا بإيرفين، أن “أنواع خلايا الدماغ المختلفة تلعب أدواراً متميزة في مرض ألزهايمر، لكن كيفية تفاعلها على المستوى الجزيئي ظلت غير واضحة.” وتضيف: “عملنا يقدم خرائط خاصة بنوع الخلية لتنظيم الجينات في دماغ مريض ألزهايمر، مما ينقل المجال من مجرد ملاحظة الارتباطات إلى الكشف عن الآليات السببية التي تدفع تطور المرض بنشاط.”
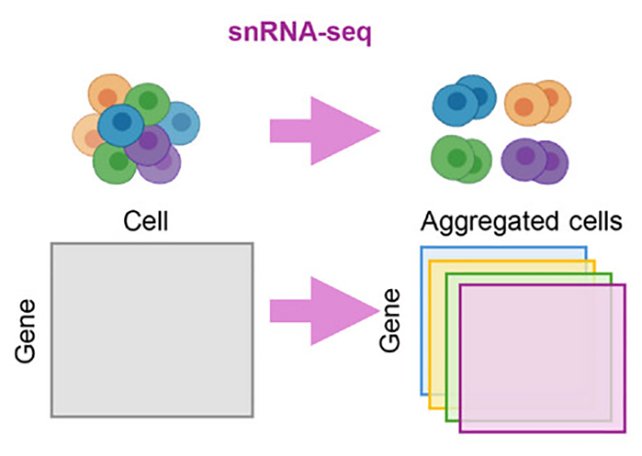
وقد اعتمد الباحثون على نظام تعلم آلي حديث يُدعى SIGNET (الاستدلال الإحصائي على شبكات تنظيم الجينات)، لتحليل مفصل لأنسجة الدماغ من 272 شخصاً توفوا بسبب ألزهايمر. ركزت الدراسة على ستة أنواع رئيسية من خلايا الدماغ: الخلايا العصبية الاستثارية، الخلايا العصبية المثبطة، الخلايا النجمية، الخلايا الدبقية الصغيرة، الخلايا الدبقية قليلة التغصن، والخلايا السلفية الدبقية قليلة التغصن. واستخدم الفريق برنامجهم للتركيز على الجينات التي سبق ربطها بألزهايمر، ولمعرفة الجينات الأخرى التي قد تؤثر فيها.
يتميز نظام SIGNET بقدرته على تحليل بيانات تسلسل الحمض النووي الريبوزي أحادي الخلية وبيانات تسلسل الجينوم الكامل، مما يتيح مقارنة نشاط جيني محدد لكل نوع من خلايا الدماغ، والصورة الأكبر للنقطة الجينية الأولية لهذه الخلايا. ويشير الدكتور داباو تشانغ، عالم الأوبئة من جامعة كاليفورنيا بإيرفين، إلى أن “معظم أدوات رسم الخرائط الجينية يمكن أن تُظهر الجينات التي تتحرك معاً، لكنها لا تستطيع تحديد الجينات التي تقود التغييرات فعلياً.” ويضيف: “بعض الطرق تفترض افتراضات غير واقعية، مثل تجاهل حلقات التغذية الراجعة بين الجينات. نهجنا يستفيد من المعلومات المشفرة في الحمض النووي لتمكين تحديد علاقات السبب والنتيجة الحقيقية بين الجينات في الدماغ.”
نقطة الضعف
أظهرت البيانات أن الخلايا العصبية الاستثارية، وهي حيوية لإشارات الدماغ، كانت الأكثر تضرراً في توصيلها الجيني المرتبط بألزهايمر. فقد تم تحديد ما يقرب من 6000 تفاعل سببي ونتائجي داخل هذه الخلايا. والأكثر من ذلك، تم التحقق لاحقاً من بيانات الخريطة الجينية مقابل عدد قليل من أدمغة بشرية إضافية مصابة بألزهايمر، والتي أظهرت أدلة على تفاعلات متسلسلة مماثلة.
هذه الاتصالات التي كانت مخفية سابقاً تمنح العلماء نظرة أكثر تفصيلاً بكثير حول كيفية تغيير ألزهايمر لتعبير الجينات في الدماغ. وهذا بدوره يفتح المزيد من الفرص لفهم كيفية تطور المرض والأساليب التي يمكن أن توقفه أو تعكسه. إن تحديد كل من الجينات المحورية المسيطرة الرئيسية والاضطراب الواسع النطاق في الخلايا العصبية الاستثارية – الضرورية للذاكرة والإدراك، والتي تتأثر بشدة بألزهايمر – يعني أن لدينا أهدافاً جديدة وأكثر تحديداً للأدوية لمكافحة ألزهايمر.
ورغم أن أي علاجات ناتجة عن هذا البحث لا تزال بعيدة المنال، إلا أن ألزهايمر مرض معقد للغاية وله العديد من المساهمات والنتائج المتداخلة، لذا فإن أي مؤشرات لمجالات البحث المستقبلية ستكون مفيدة. وعلى الرغم من دقة الدراسة، فإنها لا تثبت بشكل قاطع أن هذه التغيرات الجينية هي التي تسبب ألزهايمر. تتمثل الخطوات التالية في إدخال مقارنات مع أنسجة الدماغ غير المتأثرة بألزهايمر، لمحاولة تمييز التحولات في توصيلات الدماغ التي تعود إلى المرض وتلك التي لا تعود إليه.
يكتب الباحثون في ورقتهم المنشورة: “للمضي قدماً، سنتعمق أكثر في النتائج الحالية للتحقيق في الشبكات المتضمنة في أمراض ألزهايمر الخاصة عبر أنواع الخلايا المختلفة. ستسمح لنا هذه المقارنة بتمييز التغيرات التنظيمية المتضمنة في التنكس العصبي عن الأنشطة الخلوية الطبيعية أثناء الشيخوخة.”
وقد نُشر هذا البحث في مجلة Alzheimer’s & Dementia.