تقدم بحثي واعد في علاج إصابات الحبل الشوكي
تطوير عضويات حبل شوكي بشرية بحجم 3 مليمترات في المختبر.
أحرز باحثون تقدمًا كبيرًا نحو تطوير علاج لإصابات الحبل الشوكي التي تؤدي إلى الشلل.
في أطباق مختبرية، نجح فريق بحثي في تنمية عضويات صغيرة للحبل الشوكي البشري. بعد ذلك، قاموا بإحداث إصابات في هذه العينات وأجروا علاجًا ساعد الأنسجة على الإصلاح والتجدد.
صرح أحد المهندسين الطبيين المشاركين في الدراسة بأنهم قرروا تطوير نموذجين مختلفين للإصابة في عضويات الحبل الشوكي البشري واختبار العلاج لمعرفة ما إذا كانت النتائج تشبه ما لوحظ سابقًا في النماذج الحيوانية.
وأضاف: “بعد تطبيق علاجنا، تلاشت الندبة الدبقية بشكل ملحوظ لتصبح بالكاد قابلة للكشف، وشاهدنا نموًا في الخلايا العصبية، مما يشبه تجدد المحاور العصبية الذي رأيناه في الحيوانات. هذا يؤكد أن علاجنا لديه فرصة جيدة للنجاح لدى البشر.”
غالبًا ما تؤدي إصابات الحبل الشوكي إلى الشلل بسبب ضعف تجدد الخلايا العصبية التالفة في الجهاز العصبي المركزي. ويعزى ذلك جزئيًا إلى آليات الكبح التي تعيق نمو المحاور العصبية الجديدة وظهور الأنسجة الندبية التي يصعب على الألياف العصبية اختراقها.
في أعمال سابقة، طوّر فريق البحث مادة أُطلق عليها اسم IKVAV-PA، استخدموها لعكس الشلل لدى الفئران المصابة بإصابة حبل شوكي حادة. يكمن مفتاح هذا العلاج في الببتيدات العلاجية فوق الجزيئية – التي أُطلق عليها اسم “الجزيئات الراقصة” – والتي يمكنها أن تتطابق مع حركة المستقبلات على الخلايا العصبية لتحفيز إعادة نمو المحاور العصبية.
وأوضح أحد الباحثين في عام 2021 أن “الخلايا نفسها ومستقبلاتها في حركة مستمرة، لذا يمكن تخيل أن الجزيئات التي تتحرك بسرعة أكبر ستصادف هذه المستقبلات بشكل متكرر. وإذا كانت الجزيئات بطيئة وغير “اجتماعية” بالقدر الكافي، فقد لا تتلامس أبدًا مع الخلايا”.
تُعد النماذج الحيوانية مهمة، لكنها مجرد خطوة أولى. ورغم أن هذه الحيوانات الصغيرة يمكن أن توفر بيئة مختبرية مناسبة لاستكشاف علاج محتمل، فإن الخطوة المنطقية التالية هي اختباره في الأنسجة البشرية – ليس في أشخاص أحياء حيث قد تحدث مضاعفات، بل في كتل مزروعة من الخلايا الجذعية.
ويقول أحد الباحثين: “أحد الجوانب الأكثر إثارة في العضويات هو أنه يمكننا استخدامها لاختبار علاجات جديدة في الأنسجة البشرية. وباستثناء التجارب السريرية، فإنها الطريقة الوحيدة لتحقيق هذا الهدف.”
وهذا ما قام به الباحثون بالفعل. فباستخدام خلايا جذعية مستحثة متعددة القدرات من متبرع بالغ، قاموا بتنمية عضويات حبل شوكي بعرض 3 مليمترات وزرعوها لعدة أشهر. وخلال هذه الفترة، طوّرت العضويات الكثير من البنية الخلوية للحبل الشوكي البشري، بما في ذلك الخلايا العصبية والخلايا النجمية وطبقات الأنسجة المنظمة.
وبمجرد أن نضجت العضويات بما فيه الكفاية، تم قطع بعضها بالمشرط، بينما تعرضت أخرى لإصابة ضغط مماثلة للصدمة الساحقة التي قد تحدث في حادث. وكلا النوعين من الإصابات يمكن أن يؤدي إلى الشلل.
في كل حالة، تعرضت العضويات لموت فوري للخلايا العصبية، ونمو الندوب الدبقية التي تتشكل حول التلف في الجهاز العصبي المركزي، والتهاب، على غرار الاستجابة التي تُرى في إصابات الحبل الشوكي الحقيقية.
ويقول أحد الباحثين: “استطعنا التمييز بين الخلايا النجمية التي تعد جزءًا من الأنسجة الطبيعية والخلايا النجمية في الندبة الدبقية، والتي تكون كبيرة وكثيفة التعبئة للغاية. كما اكتشفنا إنتاج بروتيوغليكانات كبريتات الكوندرويتين، وهي جزيئات في الجهاز العصبي تستجيب للإصابة والمرض.”
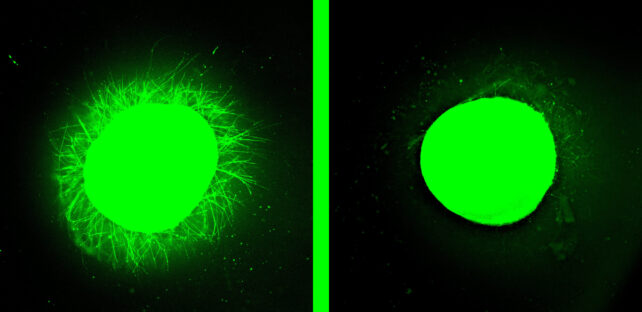
بعد ذلك، تم تطبيق سائل IKVAV-PA على بعض الإصابات، بينما عولجت إصابات أخرى بمادة تحكم لم تحتوي على الجزيئات الراقصة. وبالنسبة للإصابات التي تلقت العلاج، تحول السائل فورًا إلى سقالة، بينما حفزت الجزيئات النشطة الخلايا العصبية كيميائيًا وفيزيائيًا على إعادة النمو.
كان الفارق لافتًا. فقد أظهرت العضويات المعالجة التهابًا وتندبًا أقل بكثير من مجموعة التحكم، ونموًا أكبر بكثير للخلايا العصبية.
لا يزال الأمر على الأرجح سنوات بعيدة عن أن يصبح جاهزًا للاختبار على البشر، لكن النتائج المتسقة عبر نماذج الأنسجة الفأرية والبشرية واعدة للغاية لتطوير علاجات مستقبلية.
نُشر البحث في دورية “Nature Biomedical Engineering”.